Yuanfeng POV: Cronología actualizada de EUDAMED
La Comisión de la UE ha anunciado recientemente actualizaciones para completar e implementar EUDAMED basadas en la enmienda 2024/1860.Este artículo describe los calendarios actuales de EUDAMED y nuestro punto de vista sobre estos calendarios para ayudar a la industria a prepararse en consecuencia.
Los calendarios actuales de EUDAMED:
- La fecha límite para la primera aplicación obligatoria de los módulos funcionales EUDAMED sigue siendo el 1 de enero de 2026.Se espera que el módulo de vigilancia sea obligatorio a partir del tercer trimestre de 2026, con la plena funcionalidad de EUDAMED prevista para el segundo trimestre de 2027..
- Los módulos Actor, UDI & Devices, Certificados y Vigilancia del Mercado se encuentran actualmente bajo auditoría.La auditoría independiente del producto mínimo viable (MVP) tiene por objeto evaluar y confirmar la funcionalidad y la interconectividad de los módulos que se consideren listos para la auditoría.Se prevé que esta auditoría se complete para el segundo trimestre de 2025.
- Mandatory use of each module is to commence six (6) months after the module is declared fully functional through the independent audit and publication in the Official Journal of the European Union (OJEU)Se espera que los módulos de actor, UDI y dispositivos, certificados y vigilancia del mercado se declaren completamente funcionales al final del segundo trimestre de 2025, lo que llevará a su fecha de aplicación obligatoria del 1 de enero. 2026.
- ¿ Qué? - Se espera que los módulos Actor, UDI & Devices, Certificados y Vigilancia del Mercado se declaren completamente funcionales a finales del segundo trimestre de 2025 y sean obligatorios para el uso de la industria el 1 de enero de 2026.
- El módulo de vigilancia no forma parte de la auditoría de MVP en curso y no se declarará plenamente funcional junto con los módulos mencionados anteriormente.El calendario revisado indica que la auditoría de ese módulo se llevará a cabo entre el segundo y tercer trimestre de 2025, con el objetivo de que la fecha de aplicación obligatoria sea el segundo trimestre de 2026.
- ¿ Qué? - Se prevé que el desarrollo del módulo de Investigación Clínica/Estudios de Rendimiento (CI/PS) continúe hasta el tercer trimestre de 2026.Una auditoría para evaluar el módulo CI/PS junto con los otros cinco (5) módulos se completará una vez que se haya desarrollado el MVP CI/PS.
- ¿ Qué?
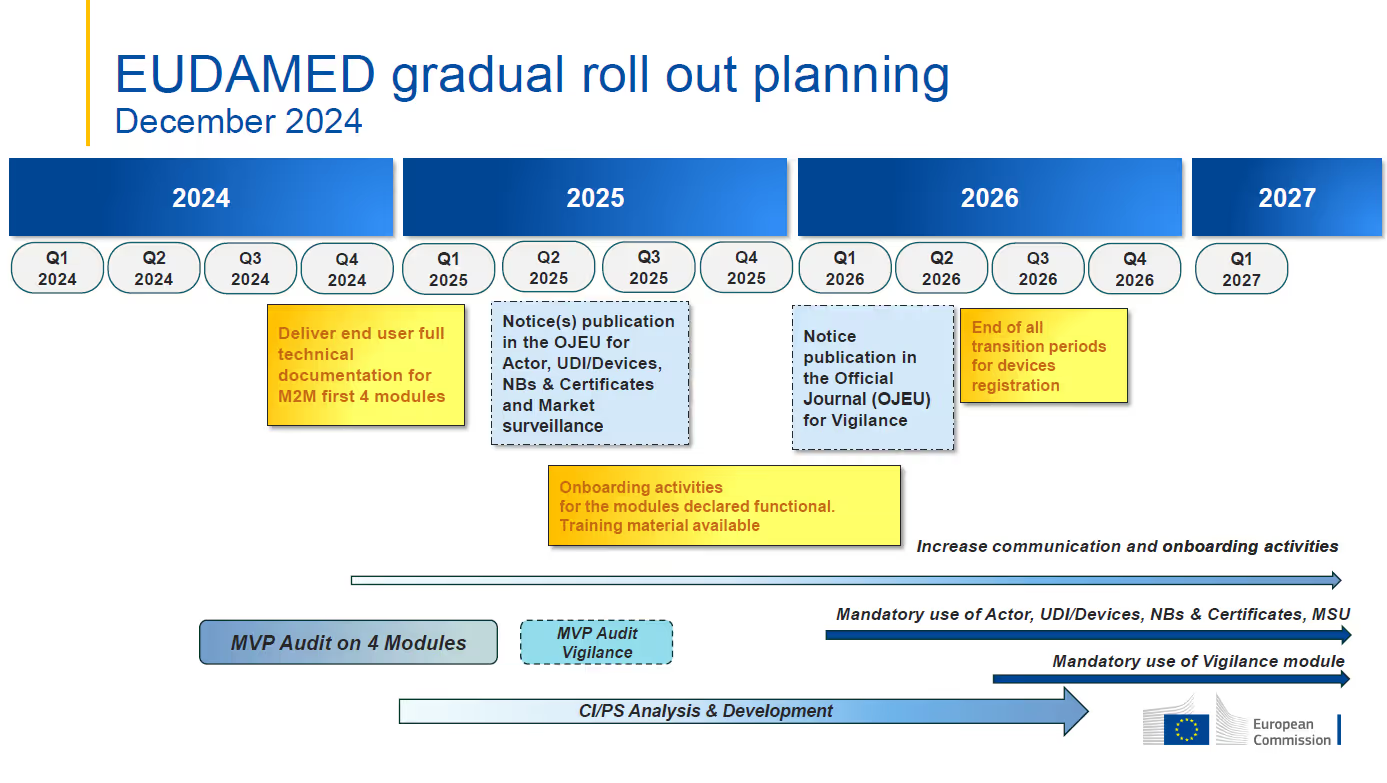
Foto cortesía delComisión Europea
La Comisión de la UE ha anunciado recientemente actualizaciones para completar e implementar EUDAMED basadas en:la enmienda 2024/1860.Este artículo describe los calendarios actuales de EUDAMED y nuestro punto de vista sobre estos calendarios para ayudar a la industria a prepararse en consecuencia.
Los calendarios actuales de EUDAMED:
- La fecha límite para la primera aplicación obligatoria de los módulos funcionales EUDAMED sigue siendo el 1 de enero de 2026.Se espera que el módulo de vigilancia sea obligatorio a partir del tercer trimestre de 2026, con la plena funcionalidad de EUDAMED prevista para el segundo trimestre de 2027..
- Los módulos Actor, UDI & Devices, Certificados y Vigilancia del Mercado se encuentran actualmente bajo auditoría.La auditoría independiente del producto mínimo viable (MVP) tiene por objeto evaluar y confirmar la funcionalidad y la interconectividad de los módulos que se consideren listos para la auditoría.Se prevé que esta auditoría se complete para el segundo trimestre de 2025.
- Mandatory use of each module is to commence six (6) months after the module is declared fully functional through the independent audit and publication in the Official Journal of the European Union (OJEU)Se espera que los módulos de actor, UDI y dispositivos, certificados y vigilancia del mercado se declaren completamente funcionales al final del segundo trimestre de 2025, lo que llevará a su fecha de aplicación obligatoria del 1 de enero. 2026.
- ¿ Qué? - Se espera que los módulos Actor, UDI & Devices, Certificados y Vigilancia del Mercado se declaren completamente funcionales a finales del segundo trimestre de 2025 y sean obligatorios para el uso de la industria el 1 de enero de 2026.
- El módulo de vigilancia no forma parte de la auditoría de MVP en curso y no se declarará plenamente funcional junto con los módulos mencionados anteriormente.El calendario revisado indica que la auditoría de ese módulo se llevará a cabo entre el segundo y tercer trimestre de 2025, con el objetivo de que la fecha de aplicación obligatoria sea el segundo trimestre de 2026.
- ¿ Qué? - Se prevé que el desarrollo del módulo de Investigación Clínica/Estudios de Rendimiento (CI/PS) continúe hasta el tercer trimestre de 2026.Una auditoría para evaluar el módulo CI/PS junto con los otros cinco (5) módulos se completará una vez que se haya desarrollado el MVP CI/PS.
- ¿ Qué?

Foto cortesía delComisión Europea
Así es como Rimsys ve el impacto de este anuncio para cada grupo de partes interesadas:
El nombre de Yuanfeng
La UDI está al frente de la mente, así como la interacción futura con el módulo de vigilancia.Rimsys continuará desarrollando la funcionalidad de UDI y vigilancia posterior del mercado independientemente de las fechas límite actualizadas.También reconocemos el impacto potencial del establecimiento de capacidades de transferencia de datos (DTX) para interactuar con EUDAMED en una capacidad de máquina a máquina (M2M).Con la publicación de los requisitos finales necesarios para el M2M DTX a EUDAMED, Rimsys está posicionado para finalizar nuestra conexión y ofrecer capacidades M2M como parte de la solución EUDAMED.
Industria/cliente
Dado que la Comisión Europea ha actualizado varias veces los plazos de EUDAMED, esperamos que la industria tenga cierta renuencia a aceptar las nuevas fechas de referencia.Esto podría retrasar la reincorporación a los preparativos de EUDAMEDSin embargo, no esperamos que la CE empuje estos plazos actualizados.Los fabricantes que no tengan un plan para presentar datos a EUDAMED para el segundo trimestre de este año deben esperar importantes desafíos para cumplir estos plazos.Con la auditoría de los módulos esperados en curso y la documentación técnica asociada publicada,Rimsys recomienda tomar medidas para organizar ahora los datos reglamentarios y enviar su información de forma anticipada a todos los módulos EUDAMED disponibles.
Comisión de la UE
La CE recomienda encarecidamente a la industria que siga desarrollando su solución y que presente datos de forma voluntaria.La posición de la Comisión es que la presentación temprana de datos dará a las empresas una ventaja al tener sus datos antes del ataque de toda la industria mundial de MedTech., todas las empresas que intentan añadir datos al mismo tiempo que EUDAMED se vuelve obligatorio.
* Nota: este artículo incluye interpretaciones y dictámenes reglamentarios de losEl nombre de YuanfengEn este sentido, el Consejo Europeo de Bruselas, en su dictamen sobre la aplicación de la directiva sobre la protección de los datos personales, propone una serie de medidas que deben adoptarse para garantizar la protección de los datos personales.

